「”学者や医者の一意見”の信頼性は、統計科学より低い」のはナゼか。知っておきたい「エビデンスレベル」と「認知バイアス」

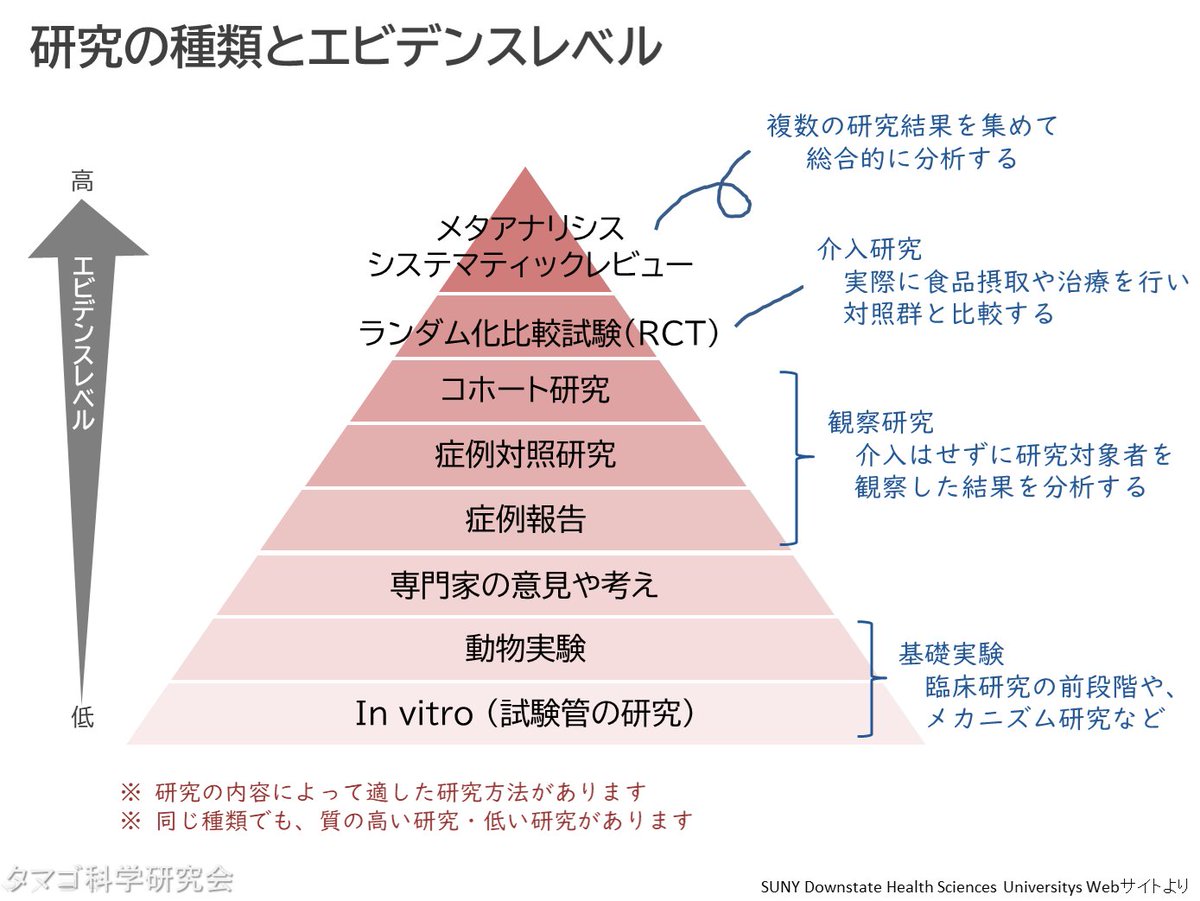
Bランク:あることを行うよう勧められる(言いきれる根拠がある )• Cランク:あることを行うように考えてもよいが、十分な科学的根拠がない(言いきれる根拠がない)• 「情報の正しさの度合い」とお考えください。 細胞・分子の実験 Dランク ピラミッドの最下層に位置しており、エビデンスのレベルは低いです。 しかし、細胞・分子の実験で効果があることは人間にも効果があると考えられるため、軽視することはできません。 「細胞・分子の実験」は食品の安全性や美容効果などについて立てた仮説を検証する研究手法です。 エビデンスレベル 弱 動物実験 Dランク マウス・ラット、ウサギ、イヌ、ネコ、サルでの動物実験がよく行われます。 私たちが使う「日用品」や「化粧品」の安全性は動物実験で確かめられます。 エビデンスレベル 弱 個人の意見 Dランク 個人は自らの「経験」に加えて「」を使い意見を主張します。 論理的推論の種類は3つあります。 演繹的推論• 帰納的推論• アブダクション 【1】演繹的推論 演繹的推論は「規則」と「前提条件」から「結論」を立てます。 【規則】赤いものはすべておいしい• 【前提条件】りんごは赤い• 【結論】だからりんごはおいしい というように。 【2】帰納的推論 帰納的推論とは「結論」と「前提条件」から「規則」を導く方法です。 【結論】AさんBさんCさんは死んだ• 【前提条件】AさんBさんCさんは人である• 【規則】人は誰しもいつか死ぬ というように。 【3】アブダクション アブダクションは「結論」と「規則」から「仮説」を立てます。 【結論】Aさんの体から汗が出ている• 【規則】体を動かすと汗が出る• 【仮説】Bさんは汗を出しているから体を動かしてきたのだろう というように。 これらの推論と自らの経験に基づいて私たちは意見を主張します。 エビデンスレベル 弱 専門家の意見 Dランク 個人と同じように 論理的推論 および 自らの経験 に基づいて意見を主張します。 ただ、専門家の方が推論に使うデータ量が豊富であるため、個人が主張する意見よりもエビデンスは強いといえます。 ここで注目するべきことは、専門家の意見だからといって、その情報が正しい、信頼性が高いわけではないということです。 専門家が細胞・分子または動物実験を根拠に使うときは、エビデンスレベルは強くないと考えます。 エビデンスレベル 中の弱 ピラミッド層の中では、専門家の意見まで人でのデータ(症例)はありません。 症例報告、ケースシリーズ Dランク 人でのデータがある層がここからです。 経験したことのある人は少ないと思いますが「治験」というアルバイトがあります。 これは人を対象にした開発中の薬の実験をする仕事を意味します。 () こうして得られた結果などが「症例報告」とされます。 エビデンスレベル 中の弱 コホート研究(観察研究) Cランク とは、ある集団を対象とした「病気の関連性」を追跡調査する研究手法です。 こちらの説明がわかりやすいかと思います。 【コホート研究】 ある特定の病気の起こる可能性がある要因・特性を考えて、対象集団(コホート)を決めます。 その要因・特性を持つグループと持たないグループとに分けて、病気の罹患や改善・悪化の有無などを一定の期間観察して、その要因・特性と病気との関連性を明らかにする研究方法。 原則として、コホート研究は介入をせず、観察のみで行われる研究。 動物で行われる実験でもコホート研究と呼ばれるそうですが、動物実験の場合はエビデンスのレベルが弱に下がると考えます。 また、コホート研究には「前向き(これから追跡)」と「後ろ向き(過去を追跡)」があります。 エビデンスレベル 中 比較臨床試験 Cランク 比較臨床試験は一方のグループには薬を飲ませ、もう一方のグループには薬を飲ませない試験のことを意味します。 その薬に「効果がある」か「効果がない」かわかります。 エビデンスレベル 強 ランダム化比較試験 Bランク 比較臨床試験をより追求した研究手法が「」です。 ランダム化比較試験は特定のグループに偏らずに、年齢や性別などに影響されない効果があるかを確かめます。 比較臨床試験とランダム化比較試験の違いは以下のとおりです。 【比較臨床試験】 年齢や性別などを指定したグループの中で薬を飲む人と飲まない人を分ける(限定的) 【ランダム化比較試験】 年齢や性別などに関わらずグループの中で薬を飲む人と飲まない人を分ける(包括的) エビデンスレベル 強 メタアナリシス Aランク ピラミッドの最上層に位置しており、最もエビデンスが強い研究手法が「」です。 メタアナリシスは下位の層で行われた結果をまとめ、 統計的に分析する手法です。 正しい情報を知るためには、情報を一面的にとらえるのではなく、多面的・多角的にとらえる必要があります。 エビデンスのレベルを考慮しつつ、さまざまな情報を比較して、自分が納得できるまで情報を検討しましょう。 情報が飛びかう世の中では、ひとつの情報を鵜呑みにせず、さまざまな情報を比較して、自分で結論を導き出すことが重要です。
次の